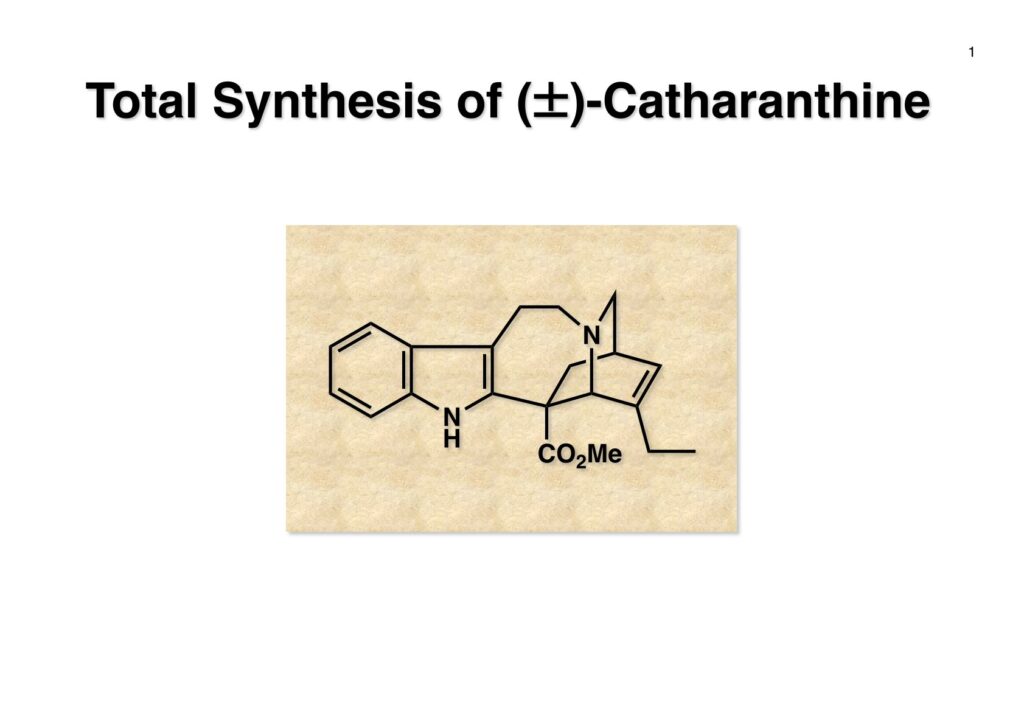
CatharanthineはVindolineの全合成を始めた流れで興味を持った化合物である。第一世代インドール合成法の試金石としてvincadifformineとはまた違うケミストリーを試す事ができると思った。アメリカ人のポスドクだったMatt Redingに最後まで頑張ってもらったが、彼はMITのBuchwald研でPh.D.を取った優秀なケミストだった。Steve Buchwaldとはハーバードで重なっていて、Mallinckrodt棟の3階が岸研、2階がKnowles研で、彼はそこの院生だった。ちょっと大きな研究費が貰えたのでSteveのところにも誰かポスドクになるような人物が居るかと尋ねたところ、丁度いい学生がいるといって紹介された。Mattの奥さん(Jennifer)は国際基督教大学(ICU)に留学しているから願ってもない機会だとSteveが推薦してくれた。その後奥さんからオフィスに電話がかかってきたが、途中まで外人と話をしているとは全く知らなかった。名前を聞いてジェニファーと言ったのでエッ!という次第。一度オフィスに来たいというので赤門まで私の秘書が迎えに行くことになったが、ジェニファーは身長が180センチくらいなので絶対に人違いしないよ、って言っていた(因みに私の秘書の田島美穂子さんは150センチちょっと)。Catharanthine全合成は第二世代インドール合成法発見の端緒となった研究で、全く一寸先のことは分からないものだ。
“Stereocontrolled Total Synthesis of (±)-Catharanthine via Radical-Mediated Indole Formation,” M. T. Reding and T. Fukuyama, Org. Lett ., 1 , 973-976 (1999).
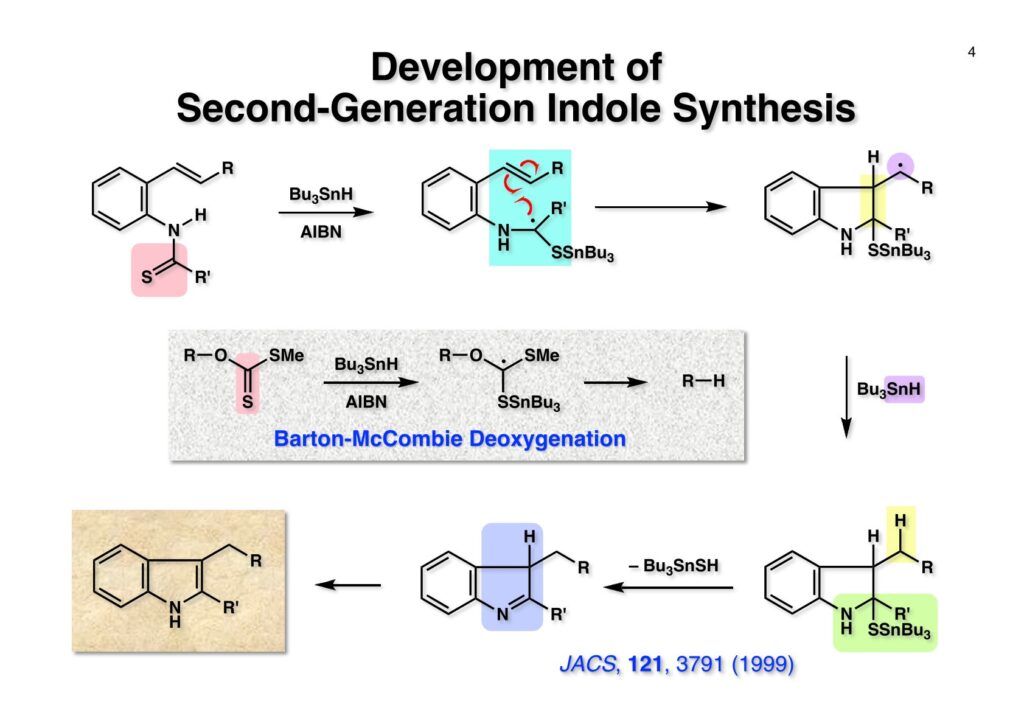
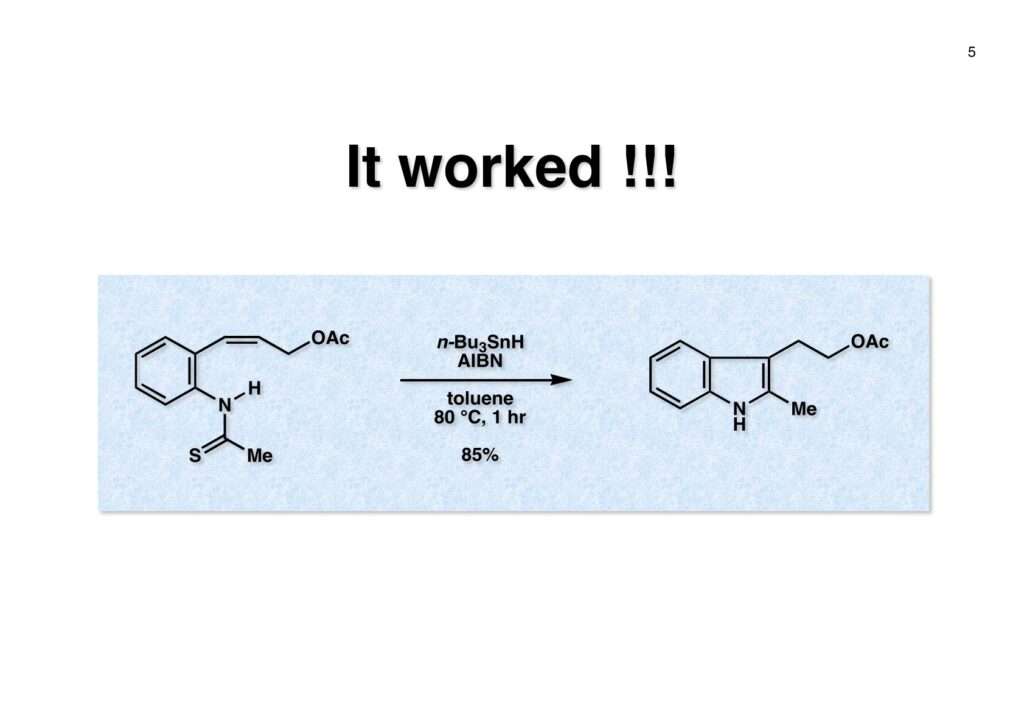
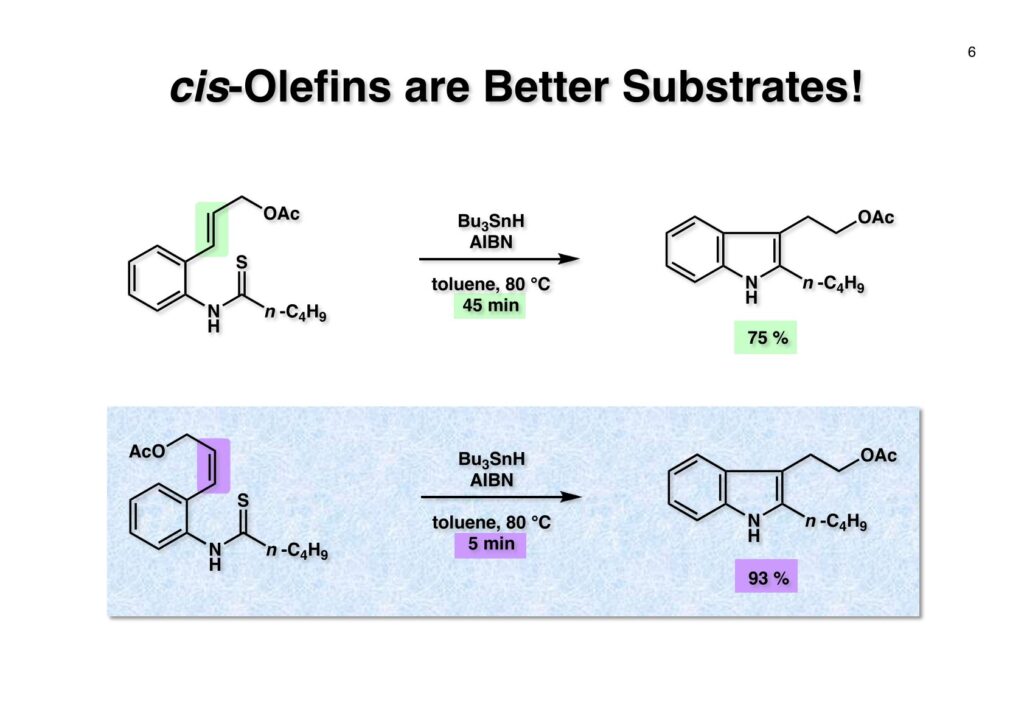
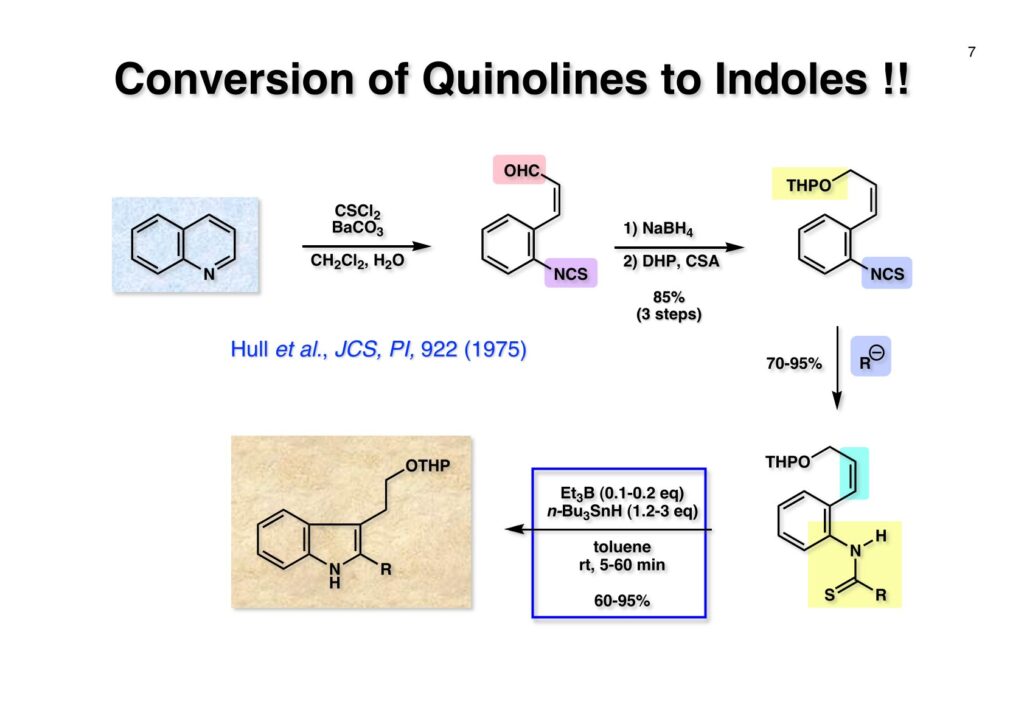
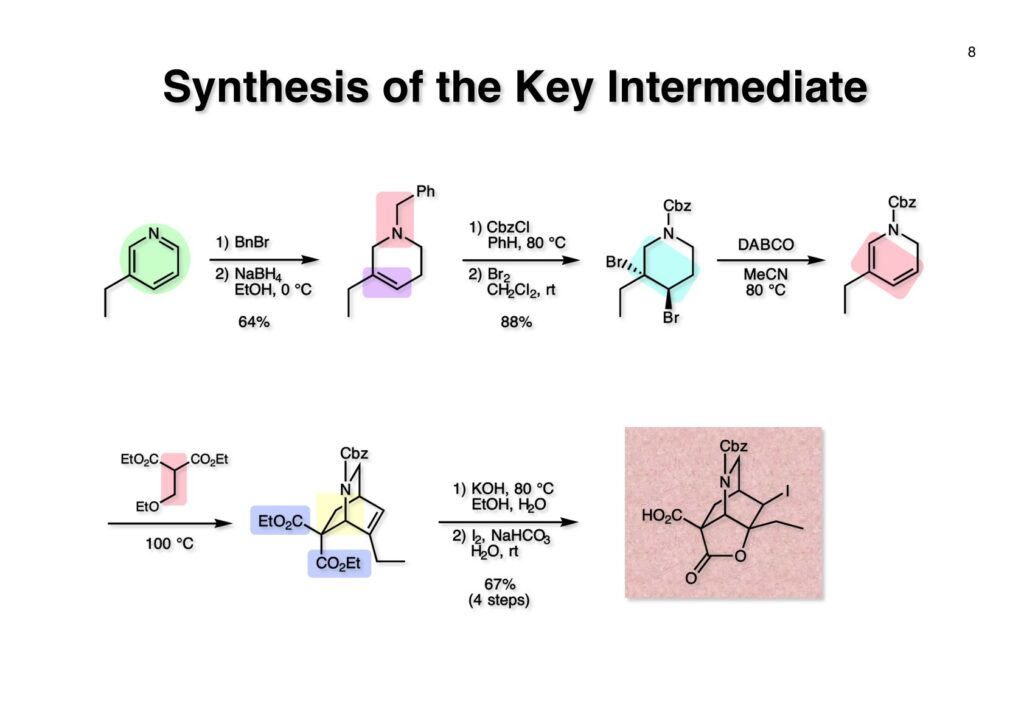
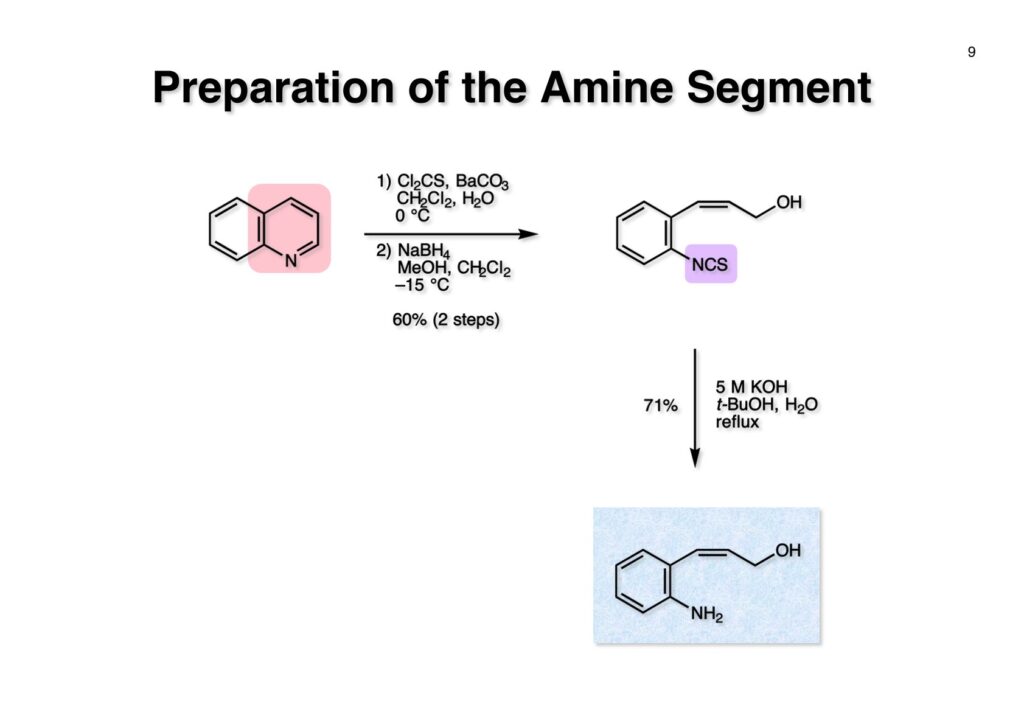
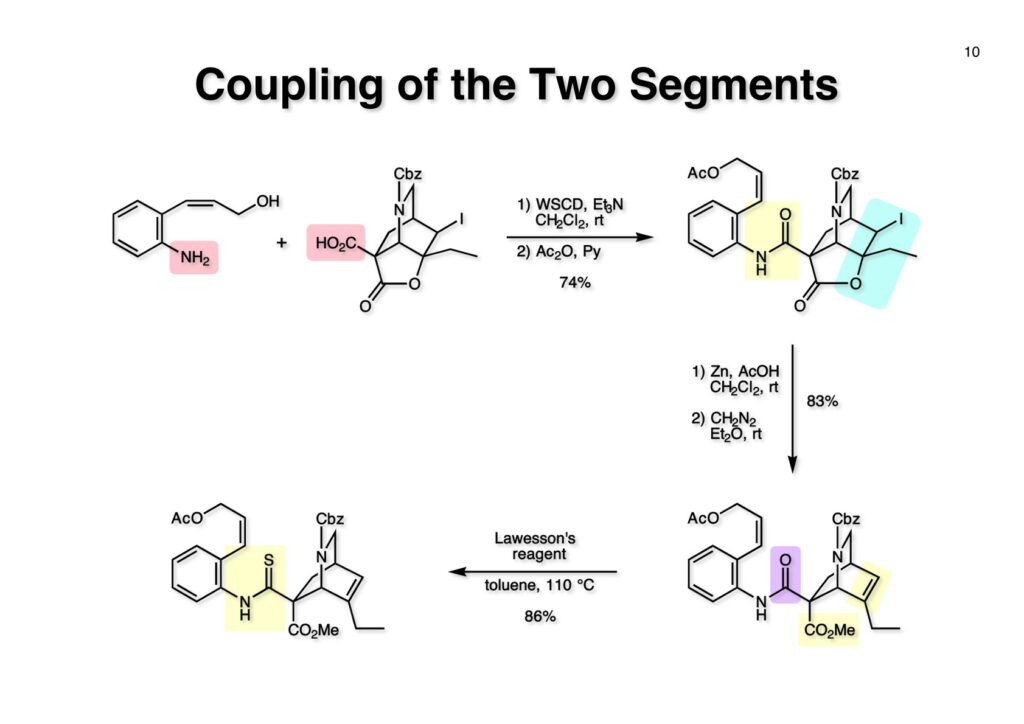
フランスのCNRS(フランス国立科学研究センター)のPotier教授とLanglois教授は天然物であるvindolineとcatharanthineからvinblastineを合成した(J. Am. Chem. Soc. , 98 , 7017 (1976))。Vindolineは我々の第一世代インドール合成法を使って全合成できたが、catharanthineの場合はsp3炭素がインドールの2位に結合しており、ベンジルブロマイドやアリルブロマイドしかsp3炭素の結合には成功していなかった。Vindolineにも青息吐息で辿り着いたので、vinblastineの全合成など夢のまた夢という状況だった。しかし、catharanthineの全合成に挑戦したおかげで第二世代のインドール合成法を開発でき、最終的にはvinblastineの完全全合成にも成功した。 とにかく何をやってもエステルのα位の炭素が2-iodoindoleの2位に結合しないので、最後の手段としてやったのが上記の実験だ。(1-1) のエステルをNaNH2で脱プロトン化し、光やFeCl2、そして金属Naを加えたりしてインドールの2位にラジカルを発生させてC-C結合を作ろうとしたが、全く目的物 (1-2) は得られなかった。因みにSRN1反応はUniversity of California, Santa CruzのJoseph Bunnett教授が発見したのだが、そのアイソトープを使った検証が面白くて印象に残っている。クロロベンゼンやブロモベンゼンを液体アンモニア中でNaNH2と反応させるとベンザインが生じてアンモニアがそれに付加したアニリンが生ずるが、ヨウ化ベンゼンはヨウ素が結合した炭素にアミノ基が結合したアニリンが生成するというものである。興味のある人は調べてみたらよい。 そこでどうすればsp3炭素をインドールの2位に入れることが出来るかを真剣に考えることにしたが、ヒントは意外に身近なところにあった。それはBarton-McCombie deoxygenationというよく知られた反応だ。これはアルコールを脱酸素化する反応で、まずアルコールをキサンテート (2-1) に変換し、Bu3SnHとAIBNでBu3Snラジカルを発生させC=S結合のSに付加させると (2-2) が生成する。ここでC-O結合が切断されて炭素ラジカルが生成し、Bu3SnHから水素を引き抜いてR-Hが得られるという反応だ。このラジカル反応をチオアミド (1-1) に適用すると (1-2) のような安定ラジカルが生成すると期待できる。このラジカルが近傍の二重結合を攻撃して速度論的に有利な5員環 (1-3) を形成すると考えられる(オーストラリア国立大学のBeckwith教授が提唱)。Bu3SnHから水素を引き抜き、さらに (3-3) からBu3SnSHが脱離するとイミン (3-2) が生成するが直ちに芳香環化してインドール (3-1) を与えると考えられる。 前ページの机上プランを実行に移したところ (1-1) は高収率でインドール (1-2) を与えた。第二世代インドール合成法の最初の例である。 次にtrans -olefin (1-1) とcis -olefin (2-1) の反応性を調べたところcis -olefinの方が反応性が高く収率も良いことが分かった。cis -Olefinは対応するアセチレンをLindlar触媒で部分還元して合成したが、過還元された飽和化合物の生成を抑制するのが面倒だった。そこで閃いたのが1990年頃にグループミーティングの反応機構問題を出すのに使っていたランカスター社のカタログに掲載されていた反応である。これはなかなか面白い反応だなーと思って頭の中に残っていた。有機化学者にとって記憶力は良いに越したことはない。えっへん! 英国マンチェスターのZeneca(現在はAstraZeneca)のケミストだったRoy Hull氏はキノリン (1-1) に水と塩基存在下でチオホスゲンを加えるとReissert型の反応が起きてcis -α,β-不飽和アルデヒドを有するイソチオシアネート (1-2) が生成することを報告した。アルデヒドとイソチオシアネートとどちらが反応性が高いのか知らなかったが、NaBH4管弦をするとアルデヒドだけが反応してアルコールになり、THPで保護して (1-3) を高収率で得た。そして更にボーナスとして、このイソチオシアネートは種々のカルバニオンと反応してチオアミド (2-2) を高収率で与えることが分かった。実はそんなの当たり前だと思っていたので、いまだに文献調査していない。これでアミドをLawesson試薬でいちいちチオアミドに変換しなくても良いことになった。勿論、(2-2) をラジカル反応の条件に付すと2位にsp3炭素が結合した様々なインドール (2-1) が合成できた。 Catharanthineに特徴的なビシクロ[2.2.2]骨格の構築から全合成を開始した。3-Ethylpyridine (1-1) の窒素をベンジル化してNaBH4還元に付すとテトラヒドロピリジン (1-2) が得られる。まず1,2-還元が起き、生成したジエナミンがEtOHによりプロトン化されて生じたイミニウム塩の1,2-還元が続くという構図だ。エナミンはaprotic solvent中ではLiAlH4によって還元されず、protic solventでNaBH4を使うと還元されることが知られている。(1-2) をCbzClとともに加熱するとベンジル基が追い出されてN-Cbz体が得られる。次に臭素を付加させてジブロモ体 (1-3) を得た。メチルアミンやベンジルアミンなどはClCO2Rと反応させて脱アルキル化することが出来るが、CbzClは熱に弱いので、脱アルキル化がもっと高い温度を必要とする時にはClCO2Ph、ClCO2CH=CH2、ClCO2CH2CCl3などが用いられる。ジブロモ体 (1-3) をアミンであるDABCOと加熱すると脱HBr化が進行してジヒドロピリジン (1-4) が得られた。これをdiethyl ethoxymethylmalonate (2-1) と加熱するとEtOHが脱離したmethylidenemalonateとのDiels-Alder反応が進行して (2-2) が得られた。Methylidenemalonateは非常に反応性が高く、malonateとHCHOとの縮合で生ずるmethylidenemalonateにmalonateが付加した二量体が主生成物となってしまう。これを避けるためmalonateとHC(OEt)3とを加熱して得られるEtOCH=C(CO2Et)2を接触還元して (2-1) を合成し、これを高温で徐々に脱エタノール化させてmethylidenemalonateを生成させるという方法が使われている。(2-2) の2つのエステルは区別が付かないので両方ともアルカリ加水分解して、iodolactonizationによって不要なカルボン酸を保護したラクトン (2-3) に変換した。 相棒のアミン (2-1) の合成はキノリン (1-1) を使いチオホスゲン、NaBH4還元で得られたイソチオシアネート (1-2) をアルカリ加水分解して (2-1) を得た。 アミン (1-1) とカルボン酸 (1-2) をWSCDで縮合し、水酸基をアセチル化してアミド (1-3) を得た。次に亜鉛-酢酸処理でヨードラクトンを還元してオレフィン-カルボン酸とし、ジアゾメタンでメチルエステル (2-2) に変換した。アミド (2-2) はLawesson試薬とトルエン中で加熱することによりチオアミド (2-1) に導いた。 チオアミド (1-1) をEt3B-Bu3SnHというラジカル反応条件に付したところ収率が20%以下となり、副反応が無視できない状態だった。これは多分に立体障害によるものと解釈しているが原因は不明である。そこで、次亜リン酸を水素源としてEt3N存在下AIBNとn -プロパノール中で加熱したところ (1-2) の収率が50%に向上した。次にアセテートを加メタノール分解し、生じた水酸基をメシレート (2-2) に変換した。残るはCbz基をPd/Cで加水素分解すれば終了だと思ったが、この触媒を使うと二重結合まで還元されてしまった。そこで大阪市大の大船泰史さんが報告した条件 (Et3SiH-Pd(OAc)2-Et3N) を適用したところ高収率でラセミ体のcatharanthine (2-1) が得られて全合成が完了した。