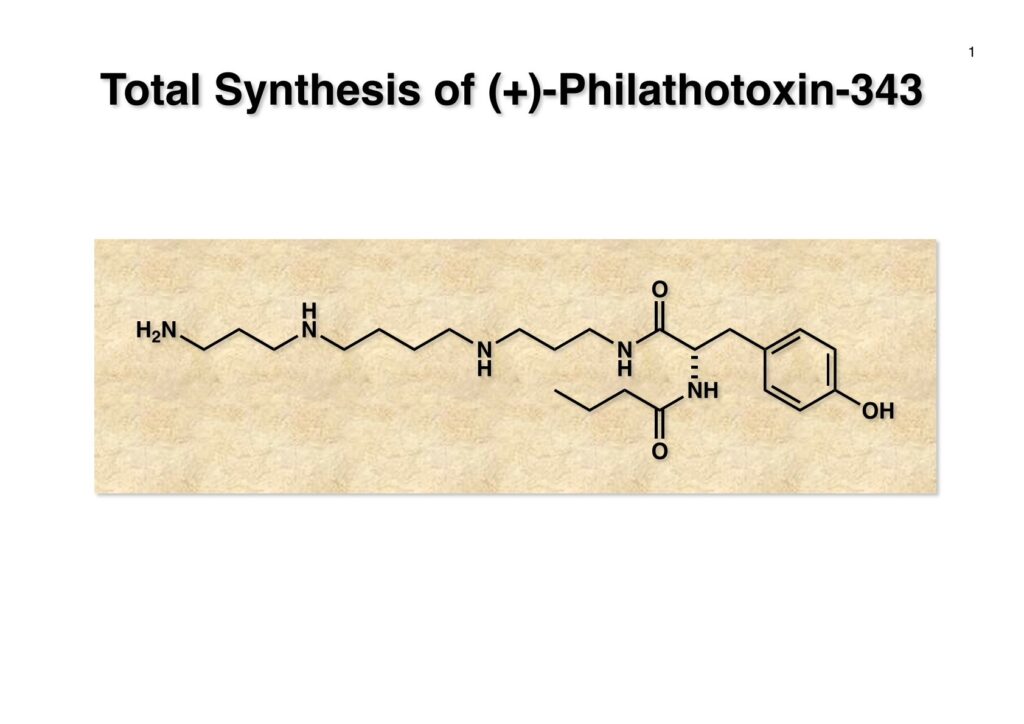
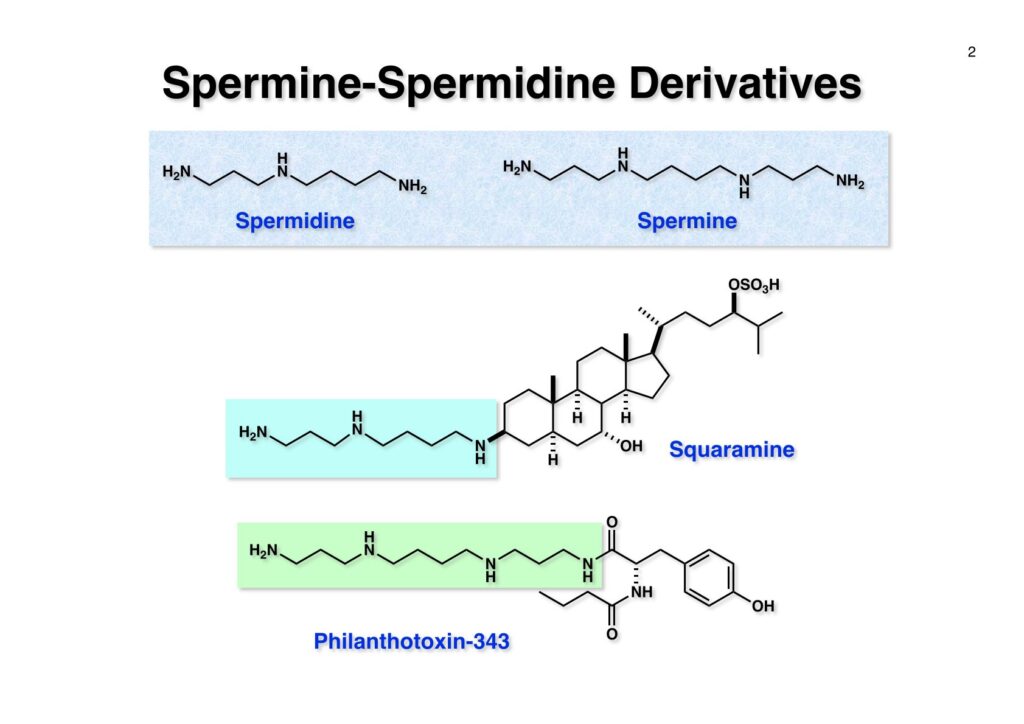
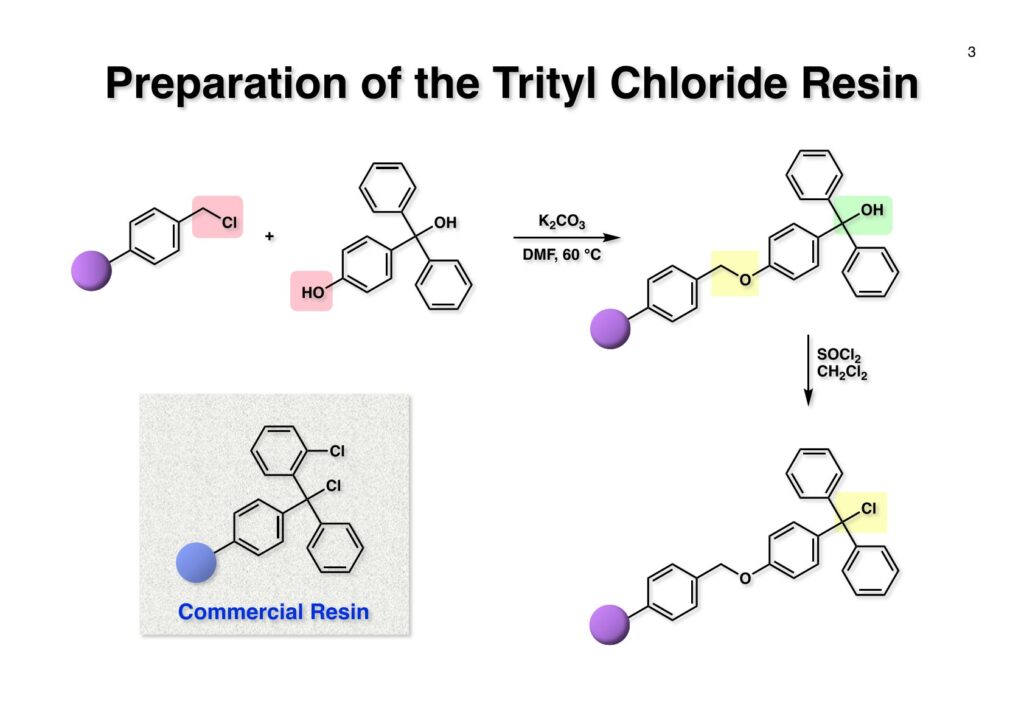
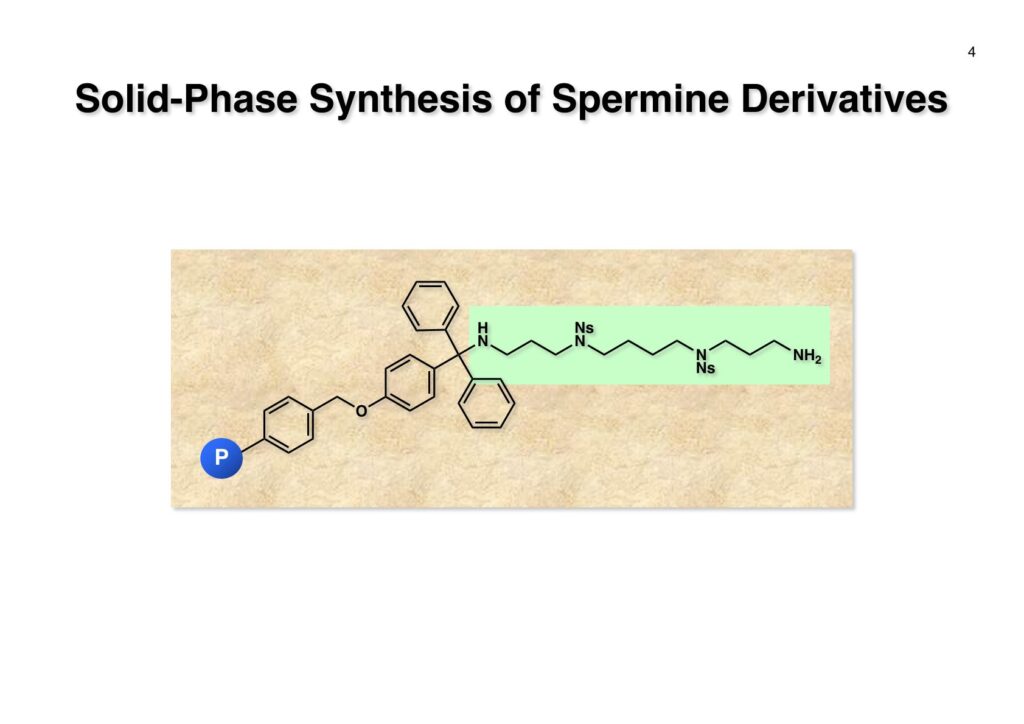
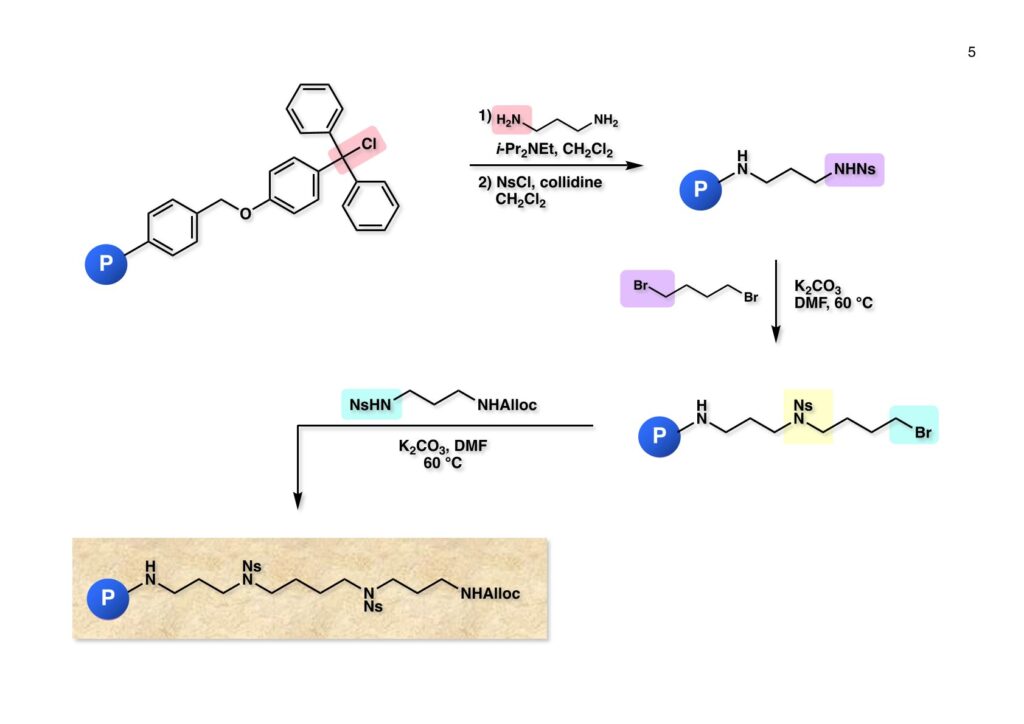
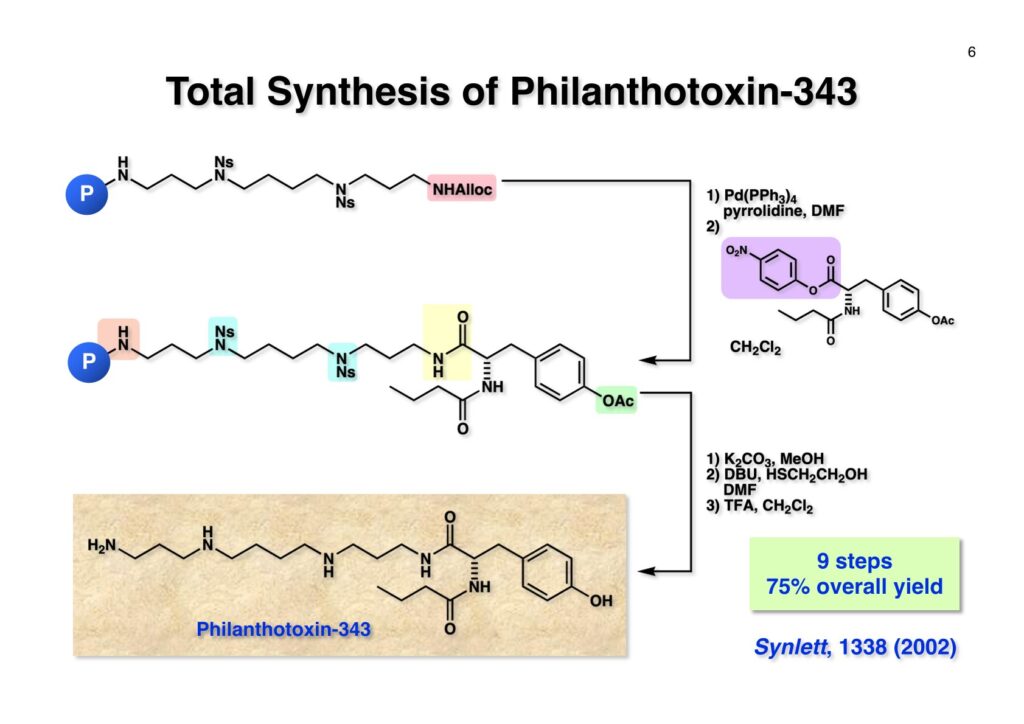
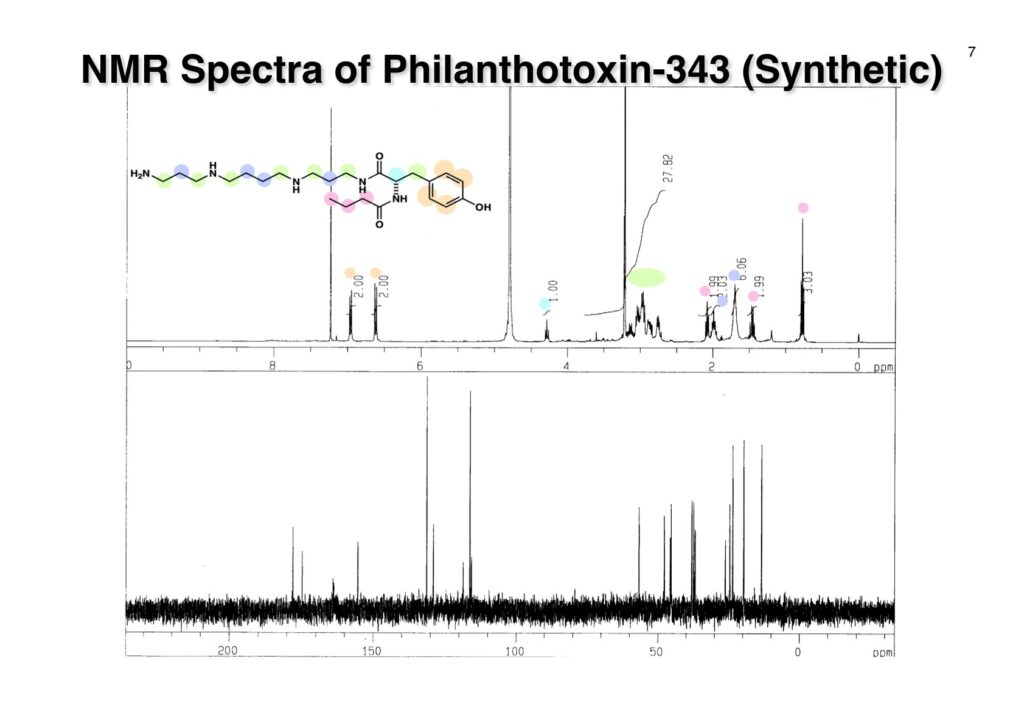
Spermineやspermidineなどのポリアミン類は細胞内特に核内に広く存在しているらしく、菅さんがポリアミンが結合した化合物は核膜を透過する性質があるので面白いと言っていた。そこで色々な化合物にポリアミンを結合させるにはポリマー上に担持されたポリアミンを用いれば良いということで、菅さん配下で現在第一三共で頑張っている小林英樹君にやってもらうことになった。私の役割は「良きにはからえ」と言っただけで、このプロジェクトは最初からうまく進行することは分かっていたし、今は亡き菅さんに代わって当ホームページに収録することにした。
“Highly Versatile Synthesis of Polyamines by the Ns-strategy on a Novel Trityl Chloride Resin,” T. Kan, H. Kobayashi, and T. Fukuyama, Synlett, 1338-1340 (2002).