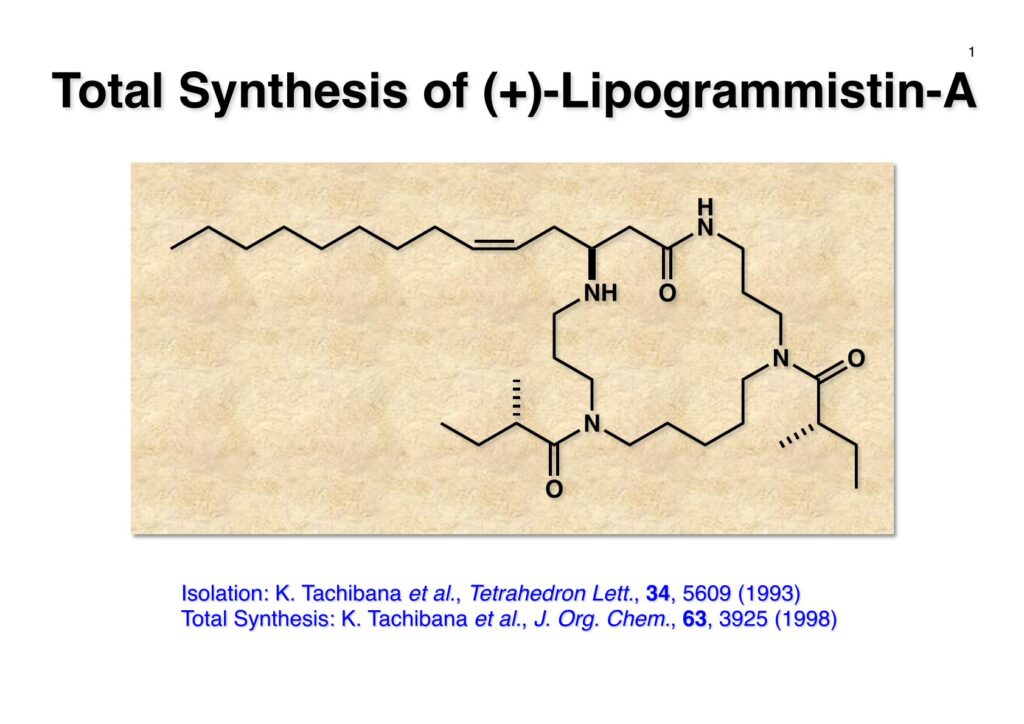
Lipogrammistin-A (LGA) はヌノサラシ科(キハッソクやルリハタなど)の魚が防御のために放出する粘液の中に含まれている化合物で、東大理学部の橘和夫先生の研究室で構造が決定され、最初の全合成も橘研で達成された。その際に菅さんのところに時々学生か助手だったか記憶にないがやってきて菅さんに色々質問していたらしい。そこでノシル基を使えばもっと良い全合成になるからやってみたいと菅さんが希望し、配下の学部生だった藤原章子に任せることにした。我が研究室に所属した女子学生はなかなか面白いのが多かったが、おそらく一番キャラが立っていたのが藤原だったかもしれない。彼女に関する面白い逸話は数々あるが、ここで明らかにすると怒られるのでやめておこう。研究室の仲間は彼女のことを「お嬢」と呼んでいたが、私はそんなの勿体無いと言って「どじょう」と呼んでいた。ただ、非常に賢くて腕も良かったことは確かである。それと、何を言ってもへこたれないので私も遠慮なしにずけずけとものを言っていた。
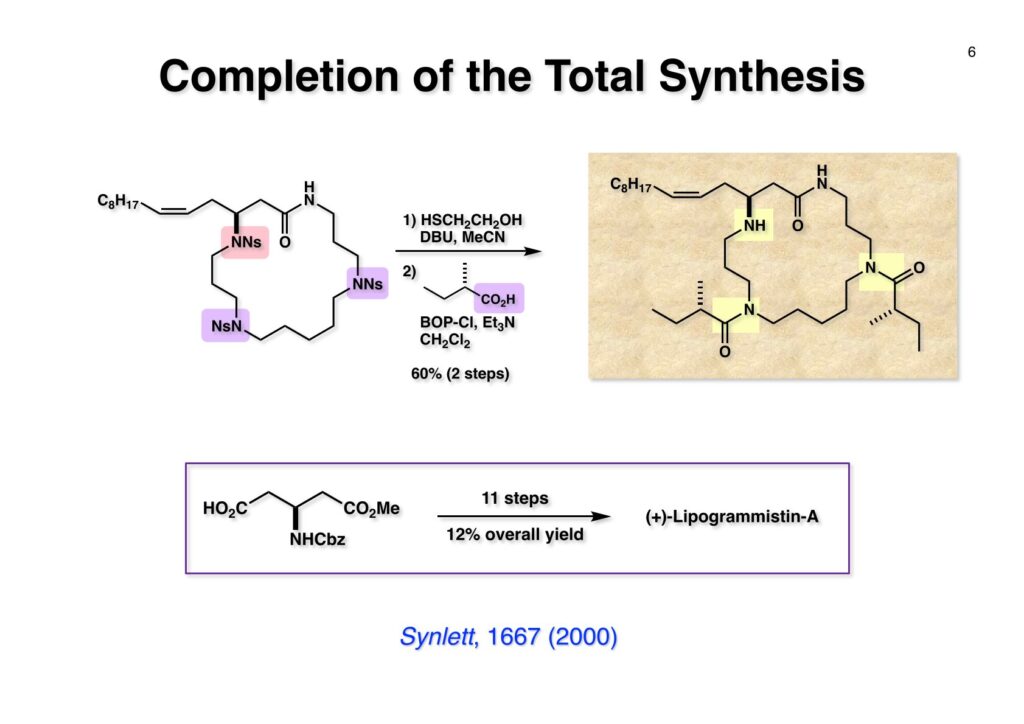
“Total Synthesis of Lipogrammistin-A: Efficient Macrocyclization with 2-Nitrobenzenesulfonamide,” A. Fujiwara, T. Kan, and T. Fukuyama, Synlett , 1667-1669 (2000).
“Efficient Macrocyclization by Means of 2-Nitrobenzenesulfonamide and Total Synthesis of Lipogrammistin-A,” T. Kan, A. Fujiwara, H. Kobayashi, and T. Fukuyama, Tetrahedron , 58 , 6267-6276 (2002).
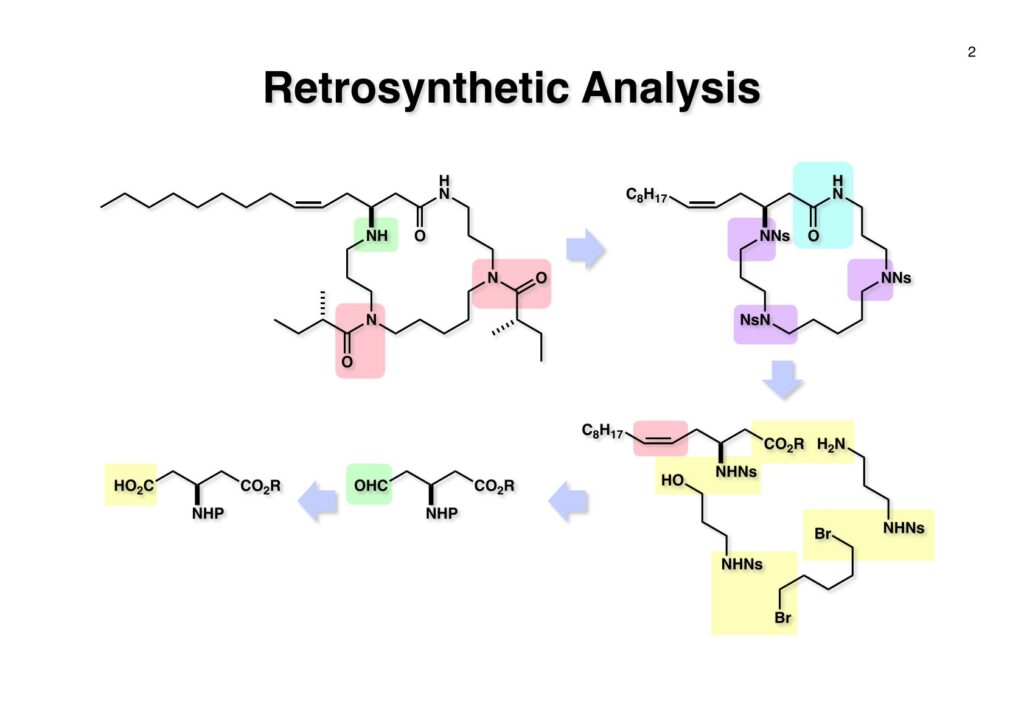
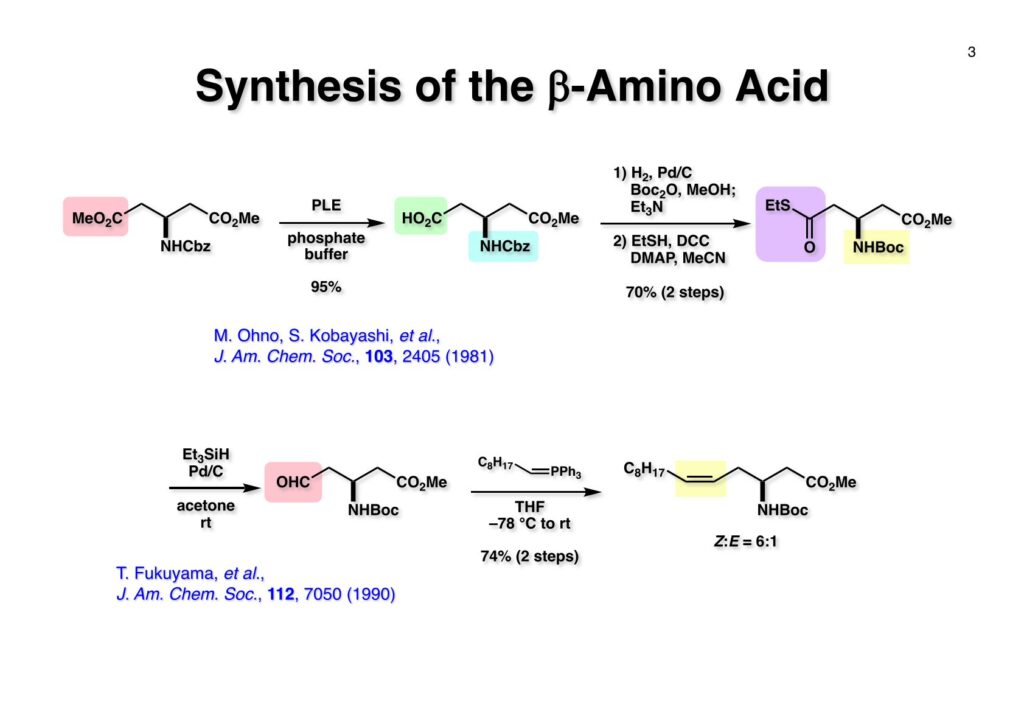
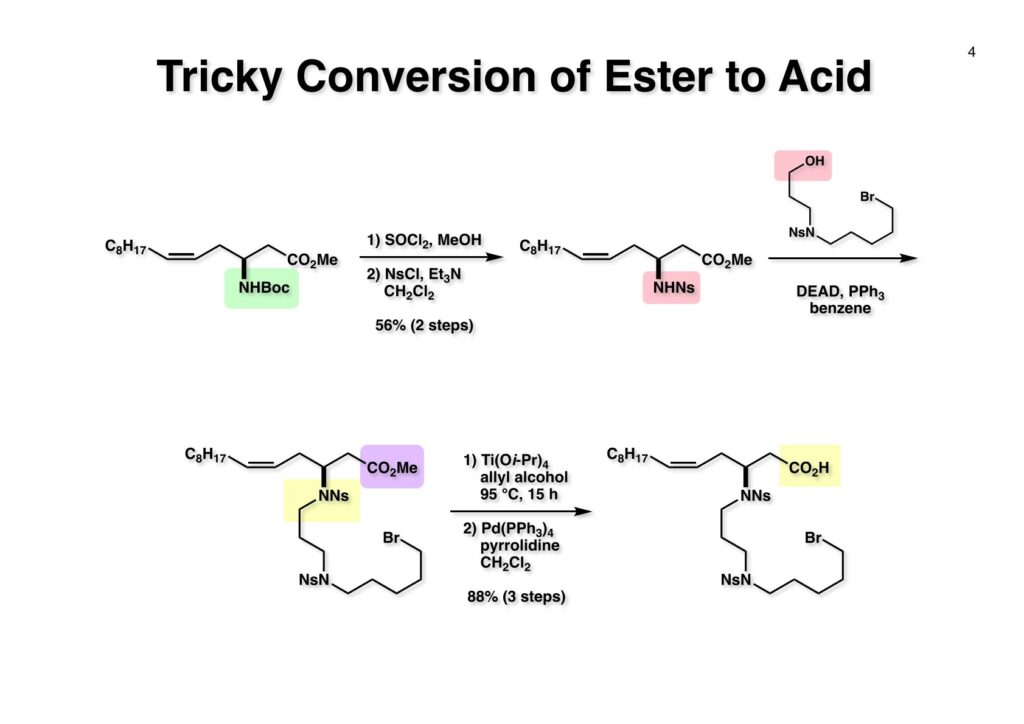
LGAの逆合成解析はそれほど難しくはない。18員環に閉環するのをどこで行うのが一番効率的か、ということはモデル実験を行って明らかにしたが、ここでは示していない。何れにしても、アミド以外のC-N結合形成はノシル基を使うことにし、マクロラクタム化を行うのはつまらないので最初から却下していた。LGA (1-1) の2つのアシル基を除去して、すべてのアミンをノシル化して (1-2) に導く。次にノシル基でN-C結合ができる箇所を切断し、アミドも加水分解することで (2-3) のような4つの部品に解体できる。cis -オレフィンはWittig反応を行えば主生成物として得られるので (2-2) のようなアルデヒドが必要となる。このアルデヒドは「福山還元」を使えばカルボン酸 (2-1) から変換できるので、最初にやるべきことは光学活性な (2-1) の合成となる。 対照的なジエステル (1-1) の酵素PLEによる選択的加水分解で光学活性なモノカルボン酸 (1-2) に変換する反応は東大薬学部の大野雅二先生の研究室から報告されていた。助教授だった小林進さんが中心になってやられた研究で、簡単に有用な (1-2) が得られた。欲を言えばCbz基でなくBoc基でも同様に高い光学純度のモノカルボン酸が得られれば、というところだがそうは行かず酵素頼みなので致し方ない。(1-2) のCbz基をBoc2O存在下加水素分解で除去し、さらにEt3Nを加えてBoc化を完結させた。次にカルボン酸をEtSH-DCCでチオエステル (1-3) に変換した。チオエステル (1-3) をアセトン中Et3SiH-Pd/Cで処理するとアルデヒド (2-1) が高収率で得られた。以前はカルボン酸をまずアルコールに還元し、さらに酸化によってアルデヒドに変換するのが常道だったが、この場合はアルコールに還元するとメチルエステルを攻撃して6員環ラクトンになってしまう恐れがある。「福山還元」を使えば直接アルデヒドに変換できるのでその心配は無用である。得られたアルデヒド (2-1) をTHF中でWittig反応を行うことでcis -オレフィン (2-2) が主生成物として得られた。おそらくDMSOを溶媒に用いた方がcis –trans 比は改善されたと思うが、ジアステレオマーの分離は簡単に行えたのでそこまではやっていない。 (1-1) のBoc基をHCl-MeOHで除去してからNsClを用いてノシルアミド (1-2) を得た。プロパノールアミンのノシル体と過剰の1,5-dibromopentaneから合成した (1-3) と (1-2) を光延反応でカップリングさせて (2-1) を得た。ところがここで問題が発生した。メチルエステルをアルカリ加水分解しようとするとノシルアミドが脱離してα,β-不飽和エステルがあっという間に生成してしまった。一方、(1-2) のメチルエステルは簡単にカルボン酸に加水分解できる。この場合はノシルアミドがアニオンになって脱離基とならないからだ。仕方ないのでちょっと遠回りをすることにした。まず、よく知られたTi(Oi -Pr)4とアルコールを使うエステル交換ではβ-脱離は起きないと思い、(2-1) をアリルアルコール中で加熱したところ、15時間かかってしまったがメチルエステルをアリルエステルに変換することができた。次にパラジウム触媒とピロリジンを使ってアリル基を除去するとカルボン酸 (2-2) が高収率で得られた。 カルボン酸 (1-1) を塩化ビバロイルと混合酸無水物にし、ジアミン (1-2) を加えてアミド (1-3) に変換した。次のCs2CO3-Bu4NIによる18員環形成はそれほど高希釈条件を使う必要がなく、確か0.1 mol/lの濃度でも高収率で目的物 (2-1) を与えた。私の想像するところではノシル基が外側を向いていて両端が近接していたのではないかと。 (1-1) の3つのノシル基はメルカプトエタノール-DBUで除去してアミンに変換した。次に光学活性カルボン酸 (1-2) とBOP-Clであしるかしたところ、2つのアミンがアシル化されたが、同じ条件では10時の位置のアミンは反応しなかった。おそらくアミドのカルボニル基との分子内水素結合と長鎖アルキル基の立体障害が原因であると思うが、これで全合成が完結した。カルボン酸 (2-1) から11段階12%通算収率で(+)-lipogrammistin-Aが合成できた。